اندازه گیری ph آب
اندازه گیری ph آب
اندازه گیری ph آب یکی از متداول ترین و مهم ترین آزمایش های انجام شده در آزمایشگاه های شیمی آب و فاضلاب می باشد که کاربرد گسترده ای دارد. از لحاظ عملی ، در هر فازی از آب و تصفیه فاضلاب که وجود دارد، کاربرد دارد. خنثی سازی با اسید و باز ، سختی گیری آب ، ترسیب ، لخته سازی ، گندزدایی ،کنترل خوردگی جاهایی هستند که به کنترل پی اچ نیاز است. پی اچ در تعیین قلیائیت و اندازه گیری کربن دی اکسید و بسیاری از معادلات اسید و باز تاثیر گذار است.

در دمای محیط ، غلظت اسیدیته و قلیائیت محلول ، شاخصی از پی اچ یا فعالیت یون هیدروژن است. اسیدیته و قلیائیت ظرفیت خنثی سازی اسید و باز آب می باشد که معمولا بر حسب میلیگرم بر لیتر کربنات کلسیم بر لیتر بیان می گردد. ظرفیت بافر، مقدار قوی بودن اسیدیته یا باز را بیان می کند و معمولا بر حسب مول بر لیتر بیان می گردد. پی اچ(PH) طبق تعریف سورن سون به صورت [+log[H تعریف می شود. شاخص شدت اسیدیته است. آب خالص به آرامی یونیزه می شود و در تعادل با محصلات یونی به صورت زیر تعریف می شود.اندازه گیری ph آب به روش فیلم زیر انجام می شود.

- [H+] = فعالیت یون های هیدروژن (مول بر لیتر)
- [OH–]= فعالیت یون های هیدروکسیل (مول بر لیتر)
- Kw = محصولات یونی آب
به دلیل معادلات آنیونی در تمام مراحل ، بهتر است محلول را رقیق کرد. واجب است استفاده کنیم از کلمه فعالیت یون ها و نه غلظت مولی. استفاده از کلمه PH ، با این فرض است که فعالیت یون هیدروژن aH+ در نظر گرفته شده باشد. معادله تقریبی در نظر گرفته شده برای مولاریته. [H+] در محلول های رقیق شده دیده می شود. شاخص لگاریتمی در دسترس است برای بیان رنج وسیعی از فعالیت های آنیونی ، معادله زیر در فرم لگاریتمی و اصلاح شده بیانگر این فعالیت است.
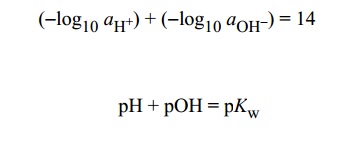
معادله بالا بیان می کند که هرچه مقدار PH افزایش می یابد ، POH کاهش می یابد و برعکس. زیرا که pKw یک ثابتی است در دمای داده شده. در دمای ۲۵ درجه سانتیگراد ، پی اچ ۷ می باشد که خنثی است. فعالیت یون های هیدروزن و هیدروکسیل معادل هستند. و برابر بودن غلظت ها در فعالیت حدودی ۷ است.











سلام
ممنون بابت مطالب مفیدتون
خواهش میکنم
این فیلمای اموزشیتون خیلی مفیده ممنونم واقعا
خواهش میکنم امیدوارم مفید بوده باشه براتون