روش اندازهگیری قلیائیت در آب
روش اندازهگیری قلیائیت در آب
قلیائیت آب ناشی از آنیونهای هیدروکسید، بی کربنات و کربنات میباشد. این یونها میتوانند به تنهایی یا همراه یکدیگر در آب ایجاد قلیائیت نمایند. یونهای دیگری مانند فسفاتها، سیلیکاتها، بوراتها میتوانند به مقدار بسیار جزئی ایجاد قلیائیت نمایند. قلیائیت آب شامل دو قسمت P و M میباشد.

قلیائیت P یا فنل فتالئین:
شامل آنیونهایی میشود که در pH بالاتر از 8/2 توسط یک اسید در حضور معرف فنل فتالئین تیتر میشوند.
قلیائیت M یا متیل اورانژ:
شامل کل آنیونهایی که در pH بالاتر از 4/3 توسط یک اسید در حضور معرف متیل اورانژ تیتر میشوند. در این جا عدد به دست آمده در حقیقت کل قلیائیت را نشان میدهد و چنانچه بخواهید قلیائیت ناشی از آنیونهای که در زیر 8/2=pH و بالای 4/3=pH تیتر میشوند را به دست آورید قلیائیت M را از قلیائیت P کم نمایید و با حرف M نشان دهید. جهت درک بیشتر مطلب میتوان به منحنی تیتراسیون زیر توجه نمایید.
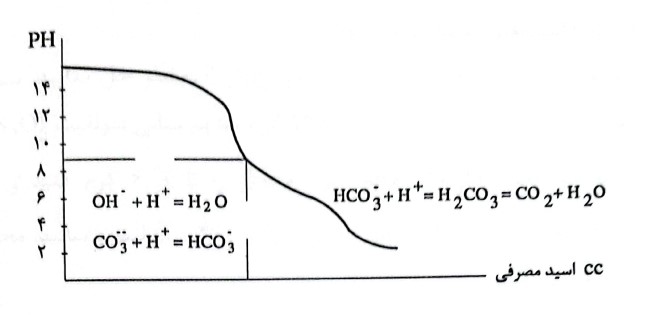
روش آزمایش:
به 100 میلیلیتر نمونه 4 قطره فنل فتالئین اضافه نمایید ( یا مقدار کمتر نمونه را با آبمقطر به حجم 100 میلیلیتر برسانید) و با کلریدریک اسید 0/1 نرمال تا تغییر رنگ محلول از گلی به بیرنگ تیتر نمایید چنانچه کمتر از دو میلیلیتر کلریدریک 0/1 مصرف شد آزمایش را با اسید رقیقتر تکرار نمایید ( قلیائیت P) جهت اندازهگیری قلیائیت M به 100 میلیلیتر نمونه دو قطره متیل اورانژ اضافه نمایید و با کلریدریک اسید 0/1 نرمال تا تغییر رنگ محلول از زرد به قرمز تیتر نمایید. تغییر رنگ را میتوان با رنگ نمونهای که شامل 100 میلیلیتر آبمقطر، دو قطره محلول متیل اورانژ و یک نوک اسپاتول پتاسیم هیدروژن فتالات میباشد مقایسه نمایید. اگر کمتر از 2 میلیلیتر مصرف شد آزمایش را با اسید دقیقتر تکرار کنید. با استفاده از فرمول زیر قلیائیت را محاسبه نمایید ( لازم به ذکر است که جهت اندازهگیری قلیائیت M میتوانید به همان نمونه اول متیل اورانژ را اضافه نمایید).

با توجه به این که کربنیک اسید و آنیونهای آن در حدود pH های 4/3 و 8/2 یک اثر بافری ایجاد مینمایند بهتر است مقدار 0/05 meq/L از فرمول شماره 2 کم گردد که برابر قلیائیت M آبهای خنثی بدون داشتن عوامل تشکیل دهنده بافر است.
روش دوم اندازهگیری قلیائیت M
در این روش میتوان از یک معرف مخلوط ( متیلن بلو و متیل رد) استفاده نمود و تغییر رنگ واضحتری را مشاهده نمود. در این روش تیتر مانند روش قبل از دو قطره معرف مخلوط و 100 میلیلیتر نمونه استفاده نمایید و عمل تیتراسیون را انجام دهید. تغییر رنگ از سبز به بنفش میباشد.
مواد و محلولهای مورد نیاز:
1- محلول متیل اورانژ: 0/5 گرم پودر متیل اورانژ را در 100 میلیلیتر آب بدون یون حل نمایید.
2- محلول 1% فنل فتالئین در اتانول: این محلول را بعد از تهیه بایستی با افزایش قطراتی از محلول سود خنثی کنید. پایان عمل خنثی شدن با ظهور رنگ ثابت قرمز بسیار کم رنگ مشخص میگردد.
3- کلریدریک اسید 0/1 نرمال یا 0/2 نرمال
4- شناساگر مخلوط: این معرف از مخلوط حجمهای مساوی از محلول 0/25 درصد متیل رد در اتیلیک الکل یا آب و محلول 17 درصد متیلن بلو در الکل یا آب به دست میآید.
نکاتی پیرامون آزمایش
معمولاً قلیائیت برحسب کلسیم کربنات بیان میشود بنابراین در فرمولهای نوشته شده عدد اکیوالان کلسیم کربنات باید ضرب شود. چنانچه بخواهید مقدار یونهای ایجاد کننده قلیائیت را اندازه بگیرید و یا به طور کلی بدانید قلیائیت ناشی از چه عواملی میباشد با استفاده از جدول زیر این امر میسر خواهد شد.
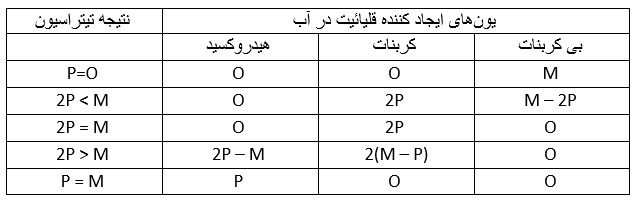
تمام مقادیر فوق بر حسب کلسیم کربنات میباشد. میتوان با ضرب نمودن آنها در ضرایب حاصل از نسبت (اکی والان یون یا نمک/اکی والان کلسیم کربنات) مقادیر را بر حسب PPm خود یون مورد نظر بیان نمود.
مثلاً جهت تبدیل قلیائیت بر حسب کلسیم کربنات بر پایه سود سوزآور PPm کلسیم کربنات را در 40/50 یا 0/8 ضرب نمایید.

شرکت دانش بنیان آبرام (آب راهبر محاسب) دارای آزمایشگاه مجهز جهت انجام تستهای شیمیایی، فیزیکی، میکروبی و فلزات سنگین انواع نمونههای آب میباشد. جهت درخواست آزمایش آب، مشاوره در زمینه آب و ارسال نمونه با ما تماس بگیرید.










